电解池教案【经典】
目前,电解池教案在当代的应用可谓是越来越广泛,电解池教案是值得我们好好学习的,现在我们就深入了解电解池教案。
电解池教案
课题:第三节 电解池
教
小熊
课
1
授课班级
教
学
目
标
知识与
技能
理解电解原理,学会书写电极反应式及总反应方程式。初步了解溶液中的微粒放电顺序,培养分析归纳知识的能力。
过程与
方法
利用惰性电极电解水和氯化铜的实验,探究电解原理。通过观察、实验、阅读资料获取信息,运用科学方法 对信息进行加工,提高科学探究能力。
情感态度
价值观
学会在思考分析过程中相互讨论,相互启发,体会到合作交流的重要性。通过电解在生产、生活中的应用实例,感受化学学科的应用价值。
重 点
理解电解原理和以电解CuCl2溶液为例得出惰性电极作阳极时电解的一般规律。
难 点
理解电解原理,惰性电极作阳极对电解产物的判断。
教学过程
[引入]氢能源是21世纪最有发展潜力的能源。氢气的制取、储存、运 输是科学家研究的重点。制取氢气的一种方法是电解水。本次课我们共同研究电解。
电解池教案
[板书]第四章第三节 电解池
一、电解原理
1、电解原理
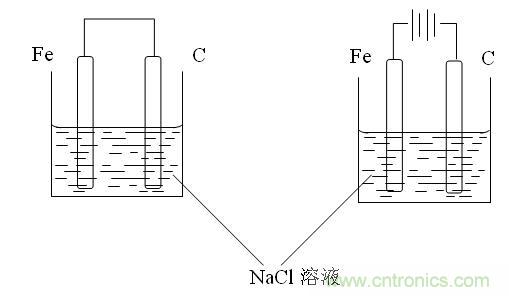
[设疑](课件展示)观察电解水的装置。接通电源电解一段时间后,分别在两电极附近滴加紫色石蕊试液,观察现象,并作出解释。
[学生总 结]两极均有气泡产生,生成氢气与氧气的体积比为2:1。滴加紫色石蕊后,与负极相连的电极 溶液变蓝色,与正极相连的电极溶液变红色。
[教师]很好,与电源负极相连的电极我们记为a极,另一电极记为b极。a极附近生成氢气,能说明哪种离子发生了反应? 发生什么反应?发生此类型反应的电极称为什么极?
[小组总 结]水发生微弱电离,H+ 在a极得到电子发生还原反应生成氢气,电化学中将发生还原反应的电极称为阴极,那么a极就是阴极。b极是水电离的OH- 失去电子发生氧化反应生成氧气,电化学中称此极为阳极。
[小结]很好,我们共同总结一下这套装置(课件展示)。
2、
阴极:与电源_____极相连,发生_________反应。
[过渡](进行电解氯化铜实验)我们知道,水的导电能力微弱,为了 增强水的导电能力,可以在水中加入电解质。在水中滴加CuCl2 溶液,请仔细观察实验现象。
[学生质疑]老师,没有连接电源,不会有现象。(连接电源后继续,出现现象后迅速停止)
[设疑]似乎没有生成氢气和氧气,描述下现象吧。
[小组总 结]阳极有气泡产生,阴极石墨上析出红色固体。
[教师]为什么呢?如何解释呢?
[猜想]阴极生成的是铜,阳极气体不能确定,可能是氧气,也可能是氯气。
[教师]如何解释呢?
[学生总结]通电时,铜离子和少量氢离子向阴极移动,氯离子和少量氢氧根向阳极移动。铜离子得电子能力比氢离子得电子能力强,所 以阴极析出铜。
[教师]非常好,如何确定阳极生成的气体是氧气还是氯气呢?电极反应式如何书写呢?
[学生总结]将湿润的碘化钾淀粉试纸放在阳极附近,若变蓝证明生成气体为氯气(重 复试验验证)。
阳极: 2Cl--2e-=Cl2↑(氧化反应)
[讲述]加入氯化铜后,电解的不在是水,而是电解质氯化铜。说明电解质溶液导电的过程就是电解质电解的过程。而氯化铜分解是 非自发的,在通电情况下可以发生,说明电解法是有力的氧化还原手段。
[结论](课件展示)
2、
4、
|
装置类别 原电池 电解池 举例 锌铜原电池 电解氯化铜溶液 形成条件 电极名称 电极反应 离子流向 电子流向 能量转变
电解池教案 [教学回顾]: [板书设 计]第四章第三节 电解池 一、电解原理 1、电解:将_______通过电解质溶液或熔融态物质,在阴极和阳极上引起________反应的过程. 2、阳极:与电源_____极相连,发生_________反应。 阴极:与电源_____极相连,发生_________反应。 4、 电解池组成 6、 电解池中的离子移动方向
|
综上所述,本文已为讲解电解池教案,相信大家对电解池教案的认识越来越深入,希望本文能对各位读者有比较大的参考价值。